Japan
サイト内の現在位置を表示しています。
ネオアンチゲンを標的としたがんワクチン療法の開発
普通論文がん免疫療法は、手術、化学療法、放射線治療に続く第4の治療法として期待されています。そのなかでもNECは、がんの遺伝子変異は患者それぞれで異なることから、個別化医療としての患者個々の腫瘍特異的変異抗原(以下、ネオアンチゲン)を標的としたワクチン治療の開発を進めています。本稿では、遺伝子解析技術及びAI技術を効果的に用い、その患者の免疫反応を強く誘導するネオアンチゲンを同定する手法を紹介します。なお、本手法を用いた個別化がん免疫療法の治験は、既に開始されています。
1. はじめに
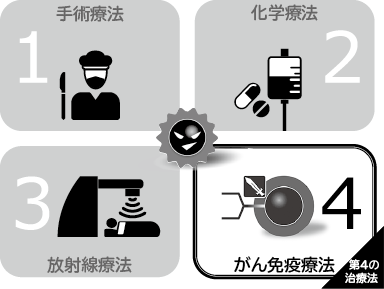
がん治療は、大きく次の3つに分けられます。それは、がんの病巣を切除する「手術療法」、抗がん剤によってがん細胞を死滅させたり増殖を抑制したりする「化学療法」、がんの病巣部に放射線を照射してがん細胞を死滅させる「放射線療法」です。いずれの方法も長い歴史のなかで発展してきたがんの治療法ですが、現在もなおそれぞれにメリット・デメリットが存在しています。近年、これらの3大治療に加え「がん免疫療法」が第4の治療法として注目されています(図1)。がん免疫療法とは、本来身体に備わっているがんに対する免疫の反応を強化し、がんの増殖・進展を制御する治療法で、全身に作用し、効果が持続し、副作用が少ない治療として期待されています。第2章でがん免疫の仕組みとがん免疫療法について概説し、第3章でNECのがんワクチン療法の取り組みを説明し、第4章でNECが取り組んでいる腫瘍特異的変異抗原(以下、ネオアンチゲン)を標的としたワクチン開発に用いているネオアンチゲン予測方法を紹介します。
2. がん免疫の仕組みとがん免疫療法
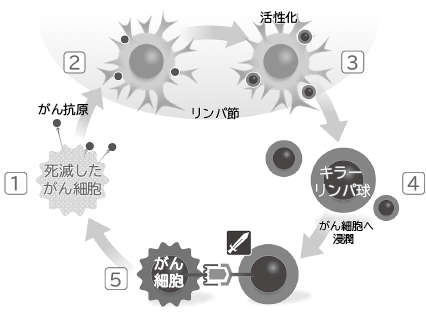
たばこや食品に含まれる発がん物質、活性酸素など、さまざまなものの影響によって遺伝子は損傷し、体内では突然変異した細胞が日々発生しています。免疫はこうした異常な細胞を監視・排除して身体を守っていますが、がん免疫逃避機構などにより、がん細胞が免疫の攻撃をすり抜けて増殖し、がん細胞に対して免疫優位な状態が保てなくなるとがんが形成されます。がん細胞に対する免疫応答の誘導を図2に示します。がん細胞はその細胞表面にがんであるという目印、すなわちがん抗原を放出しており(図2の1)、放出されたがん抗原は樹状細胞などの抗原提示細胞に貪食されます。がん抗原を貪食した抗原提示細胞はリンパ管を経由してリンパ節へ移動し、主要組織適合遺伝子複合体(Major histocompatibility complex : MHC)クラスI分子及びII分子の上にがん抗原の断片であるペプチドを載せ、T細胞に提示します(図2の2)。T細胞はMHC分子の上に提示されたがん抗原ペプチドを、T細胞受容体(T-cell receptor : TCR)を介して認識することで、活性化します(図2の3)。活性化したT細胞は、がん組織に向かって血管内を移動し(図2の4)、血管から出てがん細胞組織に向かって浸潤します。がん細胞も自身のがん抗原ペプチドをMHC分子上に提示しており、T細胞はTCRを介してこのがん抗原ペプチドとMHCの複合体を認識し、がん細胞を攻撃・排除します(図2の5)。
がん免疫療法には、体外の異物を体内に投与し免疫反応を活性化させるという免疫療法のなかでも初期の治療法である「BRM療法(免疫賦活療法)」、患者の体内からリンパ球や樹状細胞などの免疫細胞を取り出し、体外で培養し再び体内に戻す「免疫細胞療法」、がん抗原の一部を注射する「がんワクチン療法」、患者の体内から採取したT細胞にがん細胞を認識できるように遺伝子改変を行い、培養して再び体内に戻す「遺伝子改変T細胞療法」、がん細胞が免疫の働きにブレーキをかけて免疫細胞の攻撃を阻止している分子に結合し免疫抑制シグナルの伝達を阻止する「免疫チェックポイント療法」など、さまざまな種類があります。
3. NECのがんワクチン療法の取り組み
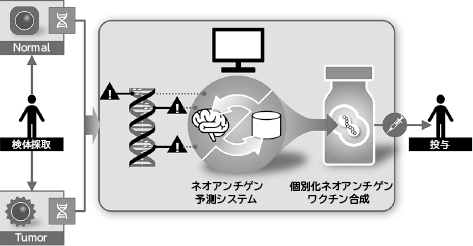
がん免疫療法のなかでもNECでは「がんワクチン療法」に注目しています。近年、次世代シーケンサーやバイオインフォマティクスの技術の発展も相まって、遺伝子変異は患者個々によって極めて多様であることが明らかとなってきました。そこで、NECは個別化医療としての患者個々のネオアンチゲンを標的としたがんワクチン療法の開発を進めています1)。NECが考えるワクチン開発プロセスは、患者から腫瘍組織及び正常組織を採取し、次世代シーケンサーによって得られた全エクソームシーケンスデータ及びRNAシーケンスデータを、独自に開発したネオアンチゲン予測システムを用いて解析することによってネオアンチゲンを選定し、ネオアンチゲンを組み込んだワクチンを合成し、患者に投与するという方法です(図3)。
4. NECが開発したネオアンチゲン予測方法
NECが開発したネオアンチゲン予測方法の処理フローを図4に示します。まず、腫瘍組織と正常組織の全エクソームシーケンスデータ(WXS)を参照ゲノム配列にマッピングし、それぞれの結果を比較することによって、腫瘍特異的な遺伝子変異を検出します。この遺伝子変異を含む9残基のペプチドを、候補エピトープとします。また、正常細胞の全エクソームシーケンスデータからHLAタイプを同定します。
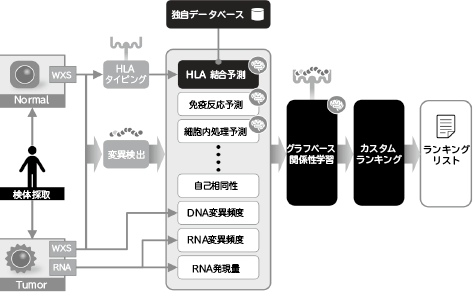
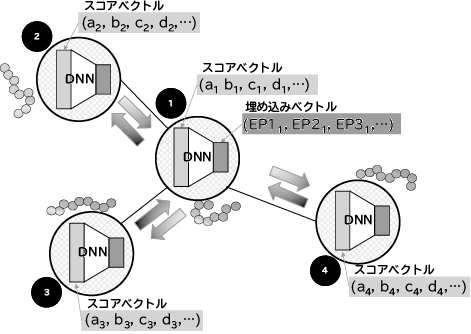
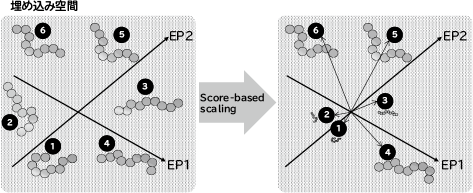
続いて、候補エピトープに対する免疫応答に関連する複数のスコアを算出します。スコアには、候補エピトープとHLA分子との結合強度を機械学習で予測した予測値2)、免疫反応を引き起こすかどうかを機械学習で予測した予測値、候補エピトープが細胞表面に提示されるかどうかを機械学習で予測した予測値、自己相同性、変異の頻度、RNA発現量などが含まれます。そして候補エピトープに対して算出された複数のスコアからグラフ関係性学習3)により総合スコアを算出します。グラフ関係性学習では、まず、候補エピトープをグラフの頂点とし、候補エピトープ間の類似性を辺で表現したグラフを作成します(図5)。次に、頂点に割り当てられた候補エピトープのスコアベクトルを、ディープニューラルネットワークを用いて次元圧縮したベクトル(埋め込みベクトル)に変換します。すべての頂点で算出された埋め込みベクトルと隣接頂点で算出された埋め込みベクトルとの誤差によってディープニューラルネットワークのパラメータを再学習します。この処理を誤差が収束するまで繰り返し、埋め込みベクトルを求めます(図6)。埋め込みベクトルを特徴量として総合免疫応答予測スコアを予測し、埋め込みベクトルの大きさを予測されたスコアの大きさに変更します(図7)。そして、埋め込み空間からスコアが大きく多様性に富んだエピトープを順に選択し、ワクチン候補を選定します。

5. おわりに
本稿では、がん免疫の仕組みとがん免疫療法、NECのがんワクチン療法の取り組み、及びNECが開発したネオアンチゲン予測手法について述べました。本手法は個別化がんワクチンだけでなく、新型コロナウイルス感染症(COVID-19)に対するワクチン設計にも応用可能です4)。
本手法を用いた個別化がん免疫療法の治験は、既に開始されています。今後は、治験期間に蓄積するデータを検証し、どのような患者に有効なのか、有効な場合、いつまで投与を続ければいいのかなどの治療計画に役立つバイオマーカーの探索も視野に入れています。本治験が成功し、がんワクチンが医薬品として承認され、多くの患者に届けられることを願いつつ、今後も創薬事業に取り組んでまいります。
参考文献
- 1)
- 2)Kuksa Pavel P. et al.:High-order neural networks and kernel methods for peptide-MHC binding prediction,Bioinformatics,Volume 31,Issue 22,pp.3,600-3,607,2015.7
- 3)Duran Alberto Garcia, Mathias Niepert:Learning graph representations with embedding propagation,NIPS'17 Proceedings of the 31st International Conference on Neural Information Processing Systems ,pp.5,125-5,136,2017.12
- 4)
執筆者プロフィール
AI創薬事業部
シニアマネージャー
博士(工学)
AI創薬事業部
主任
AI創薬事業部
NEC Laboratories Europe
Systems and Machine Learning
シニアリサーチャー
Ph.D.
